Le cerveau d’un patient atteint de la maladie d’Alzheimer est caractérisée par deux types de lésions : les plaques d’amyloïde et les dégénérescences neurofibrillaires.
Les plaques d’amyloïde sont situées autour des neurones et sont composées de protéines amyloïdes qui s’accumulent et s’agrègent pour former des plaques.
Les dégénérescences neurofibrillaires (DNF) sont formées d’une protéine appelée tau. Cette protéine apparaît sous une forme anormale dans la maladie d’Alzheimer, ce qui conduit à son accumulation à l’intérieur des neurones sous la forme de filaments qui finissent par ‘étouffer` les neurones.
En résumé il existe deux types de lésions dans la maladie d’Alzheimer :
1. Les plaques amyloïde sont situées autour des neurones.
2. Les DNF situées à l’intérieur des neurones.
Ces deux formes de lésions sont responsables de la mort des neurones et de la perte des synapses dans des régions responsables d’un bon fonctionnement cognitif (mémoire, apprentissage, fonctions exécutives).
Lorsque ces régions sont touchées, le patient ne peut plus mémoriser et un diagnostic de démence de type Alzheimer est posé.
La quantité de plaques amyloïde et de DNF augmente avec la sévérité de la maladie.
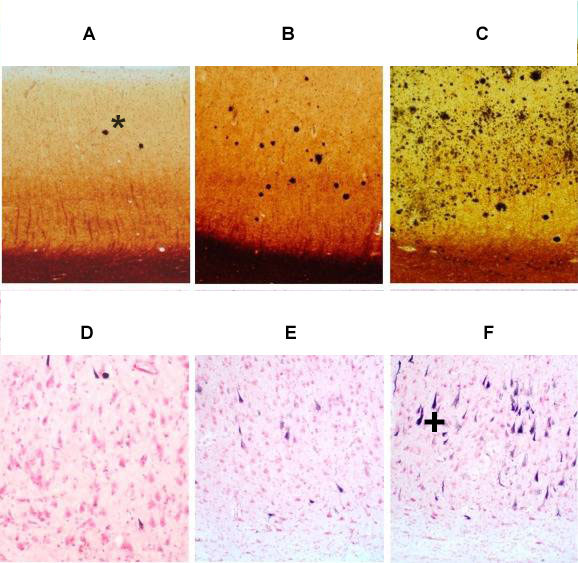
Légende : accumulation de plaques d’amyloïde (représentées par *) et de dégénérescences neurofibrillaires (représentées par +) en fonction de la sévérité de la maladie d’Alzheimer : stades précoce (A et D), modéré (B et E) et sévère (C et F) de la maladie.
Les lésions apparaissent avant les premiers symptômes d’Alzheimer
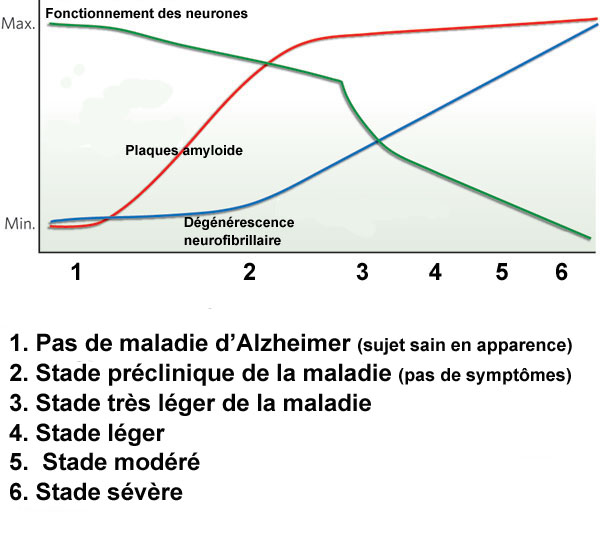
Les études cliniques ont permis de s’apercevoir que les plaques amyloïdes et les DNF s’accumulent bien avant (environ 10 à 15 ans) que la perte des neurones soit suffisamment marquée pour provoquer les premiers symptômes de la maladie d’Alzheimer.
Légende : évolution des lésions de la maladie d’Alzheimer (plaques amyloïde et DNF) en fonction de la mort neuronale.
Cela explique la raison pour laquelle les médicaments actuellement prescrits (donépezil, galantamine, rivastigmine, mémantine) ne guérissent pas la maladie d’Alzheimer.
Les études cliniques visant à bloquer la formation des plaques séniles n’ont apporté jusqu’à présent aucun résultat encourageant, d’où l’importance de mettre l’accent sur:
– la prévention (bonne alimentation, exercice physique, activité mentale) et ;
– l’identification à un stade très précoce des personnes à risque susceptible de développer la maladie d’Alzheimer.
L’utilisation de marqueurs biologiques pourrait permettre de mesurer de manière plus fiable les troubles cognitifs et ses causes lorsqu’ils ont combinés aux tests neuropsychologiques et neurologiques.
Ces marqueurs pourraient surtout permettre aux cliniciens d’identifier et de traquer la pathologie bien avant l’apparition des déficits cognitifs.
Quels sont ces marqueurs?
Plaques amyloïde
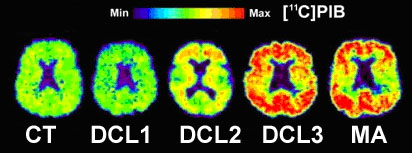
Le traceur le plus largement utilisé pour marquer les plaques amyloïdes est le Pittsburgh Compound B-carbone 11 (11C-PIB). Plusieurs études cliniques ont déjà montré qu’il est possible de séparer nettement par tomographie par émission de positons (TEP) les sujets âgés sains des patients atteints de troubles cognitifs légers (DCL) et des malades atteints de maladie d’Alzheimer. En effet la quantité de traceur est plus importante dans les zones où se concentrent les plaques amyloides. De plus, il semble possible de distinguer parmi les patients DCL ceux qui vont évoluer vers la maladie d’Alzheimer de ceux qui n’évolueront pas. Le PIB étant marqué au carbone 11 qui a une courte demi-vie, il est difficile d’envisager son utilisation dans le cadre de la clinique. C’est pourquoi des traceurs marqués au fluor 18 sont en cours de validation. Un de ces traceurs, le 18F-FDDNP, est déjà testé chez les différentes catégories d’individus (sujets sains, DCL et Alzheimer).
Légende : capture de la sonde (11C-PIB) observée chez des patients sains (CT), souffrant d’un déficit cognitif léger de sévérité croissante (DCL1, DCL2 et DCL3) ou de la maladie d’Alzheimer (MA).
Neuro-inflammation
Comme beaucoup de processus de mort neuronale, la maladie d’Alzheimer s’accompagne d’une neuro-inflammation (c’est-à-dire d’une réaction inflammatoire affectant les neurones) qui se traduit par une surexpression des récepteurs aux benzodiazépines périphériques. Ces derniers sont donc une cible intéressante pour suivre l’évolution de la maladie. Un marqueur biologique marqué au carbone 11 (appelé 11C-PK11195) a été testé chez l’homme, mais présente des difficultés d’utilisation liées à la courte période du carbone 11 (11C). De nouveaux traceurs marqués au fluor 18 sont en cours d’essai.
Niveaux de protéines amyloide et tau
Plusieurs études indiquent que les niveaux de protéines amyloïde et tau dans le liquide céphalorachidien (LCR; liquide dans lequel baignent le cerveau et la moelle épinière) de sujets âgés peuvent prédire l’apparition d’une démence chez des sujets qui ne présentent pas encore de symptômes. Ainsi, plus de 80% d’individus âgés ayant de faibles niveaux de protéine tau et des niveaux élevés de protéines amyloïde ne présenteront aucun déficit cognitif dans les quatre prochaines années.
En revanche, seulement 30% de sujets resteront sains dans les quatre prochaines années s’ils présentent des niveaux élevés de tau et de faibles niveaux d’amyloïde dans le liquide céphalorachidien.
Les faibles taux d’amyloïde dans le LCR de patients s’expliqueraient par le fait que les plaques amyloide (qui s’accumulent donc dans le cerveau des patients Alzheimer), empêchent l’amyloïde de passer dans le LCR.