Leucopathie
Commentaires fermés sur LeucopathieLa leucopathie est une atteinte neurologique se caractérisant plus précisément par une lésion de la substance blanche quelque soit la cause de la lésion.
Leucopathie vient du grec leuco = blanc et de pathos = maladie.
On parle également de leucoencéphalopathie.
Elle s’accompagne la plupart du temps de problèmes de circulation sanguine dans le cerveau. Ce dernier est alors mal irrigué par les artérioles et les capillaires. On parle de leucopathie (ou leucoencéphalopathie vasculaire).
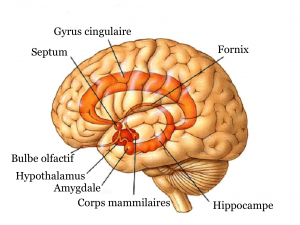
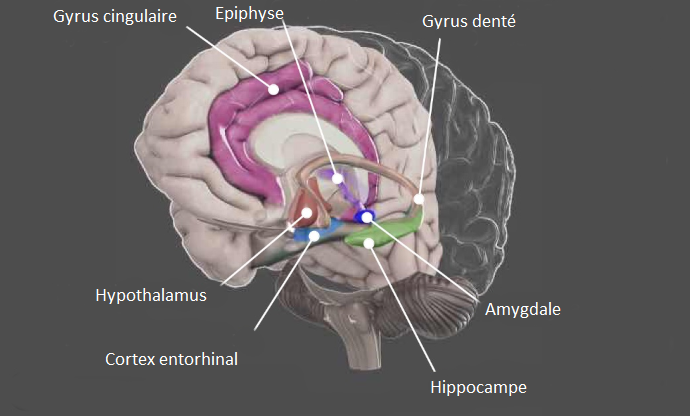
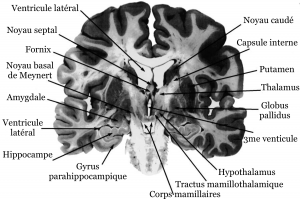
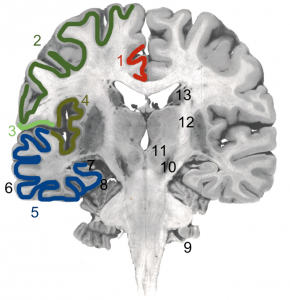
Qu’est-ce-que la substance blanche ?
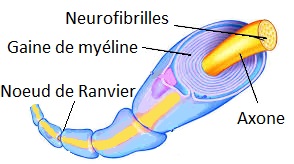
La substance blanche fait partie du tissu nerveux composé des axones. Les axones sont les prolongements des neurones et permettent le passage de l’information entre deux neurones par la propagation de l’influx nerveux.
Ils sont entourés d’une gaine de myéline, une sorte de couche de lipides (cholestérol, phospholipides, glycolipides).
La substance blanche est donc impliquée dans la transmission de l’information dans le système nerveux central et le cerveau en particulier.
La gaine de myéline est donc endommagée dans la leucopathie.
Classification des différents types de leucopathie
On distingue les leucopathies acquises et celles qui sont héréditaires.
Les leucoencéphalopathies héréditaires ayant une cause génétique sont ensuite classés en fonction du gène qui est en cause (ce gène mute et cette mutation est à l’origine de la lésion de la substance blanche).
Quant aux leucopathies acquises, elles sont classées en différents groupes selon leurs causes sous-jacentes:
- inflammatoire et non-infectieuse.
- inflammatoire et infectieuse.
- hypoxique et ischémique. (exemple la maladie de Binswanger)
- traumatique.
- toxique et métabolique.
Exemples de maladies qui entraînent une leucopathie
Il existe plusieurs maladies qui entraînent des dommages de la substance blanche:
Sclérose en plaques
La sclérose en plaques est une maladie neurologique caractérisée par une inflammation des neurones (appelée neuro-inflammation), provoquant notamment des troubles visuels et moteurs.
Leucoencéphalopathie multifocale progressive
La leucoencéphalopathie multifocale progressive est une maladie virale rare et souvent fatale caractérisée par des lésions progressives ou une inflammation de la substance blanche à plusieurs endroits (multifocale). Elle est causée par un virus qui est normalement maintenu sous contrôle par système immunitaire. Ce virus est normalement inoffensif sauf en cas de système immunitaire affaibli (observé dans des maladies telles que le SIDA, les leucémies et la maladie de Hodgin). En général, le taux de mortalité de la LEMP se situe entre 30 et 50% au cours des premiers mois et les personnes qui survivent gardent des handicaps neurologiques.
Leucoaraïose
Une leucoaraïose, accompagnée également d’une neuro-inflammation.
Maladie d’Alzheimer
La maladie d’Alzheimer est la forme la plus importante de démence et s’accompagne d’anomalies de la substance blanche.
Leucoencéphalopathie toxique
C’est une affection rare caractérisée par des lésions progressives de la substance blanche. Elle est provoquée par une toxicomanie, des toxines environnementales ou des médicaments chimiothérapeutiques. La sévérité de la leucoencéphalopathie toxique varie par ailleurs selon les patients, la durée d’exposition et la concentration de l’agent toxique. La maladie est peut-être réversible dans de nombreux cas lorsque l’agent toxique est éliminé.
Syndrome de leucoencéphalopathie postérieure réversible
Le syndrome d’encéphalopathie postérieure réversible (SEPR) est un syndrome caractérisé par des maux de tête, de la confusion, des convulsions et une perte de vision. Elle peut avoir plusieurs causes, notamment l’hypertension maligne et certains traitements médicaux. Sur l’imagerie par résonance magnétique (IRM) du cerveau, on observe des zones d’œdème (gonflement). Les symptômes ont tendance à disparaître après un certain temps, bien que des modifications visuelles subsistent parfois.
Leucoencéphalopathie hypertensive
La leucoencéphalopathie hypertensive se réfère à une dégénérescence de la substance blanche du cerveau suite à une augmentation soudaine de la pression artérielle. Les personnes peuvent présenter une augmentation soudaine de la pression artérielle, un état confusionnel aigu, des maux de tête, des vomissements et des convulsions. Des hémorragies rétiniennes peuvent être présentes lors de l’examen. La leucoencéphalopathie hypertensive peut entraîner une ischémie cardiaque.
A ces leucoencéphalopathies acquises s’ajoutent celles qui ont pour origine une mutation génétique :
Leucoencéphalopathie mégalencéphalique avec kystes sous-corticaux. Cette forme de leucopathie a une cause génétique. Elle se caractérise par des kystes (cavités de petites tailles) sous-corticaux. Elle appartient à un groupe de maladies appelées leucodystrophies. (également appelée maladie de Van der Knaap).
Leucoencéphalopathie héréditaire diffuse à sphéroïdes axonaux
La leucoencéphalopathie avec sphéroïdes neuroaxonaux est une forme particulière de leucoencéphalopathie. Les sphéroïdes sont des gonflements axonaux discontinus caractérisés par l’absence de gaines de myéline. Ils causent une régression cognitive progressive et motrice. C’est une maladie d’origine génétique, suivant un profil autosomique dominant. Elle se présente généralement pendant l’enfance, mais elle peut aussi apparaître à l’âge adulte, auquel cas elles peut présenter des caractéristiques neurologiques semblables à celles de la sclérose en plaques.
Leucoencéphalopathies vasculaires héréditaires
Elles incluent la maladie de CADASIL (mutation du gène NOTCH3), la maladie de CARASIL (mutation du gène HTRA1) et l’angiopathie amyloïde cérébrale. Dans le cas du CADASIL, il existe des antécédents familiaux d’accidents vascualires cérébraux.
Childhood Ataxia with diffuse Central nervous system Hypomyelination
Ce syndrome a été initialement décrit chez l’enfant. Les formes adultes
sont cependant de plus en plus reconnues. Les symptômes neurologiques sont très variables (ataxie cérébelleuse, symptômes psychiatriques et démentiels). C’est une maladie neurologique autosomique récessive, provoquées par la mutation de gènes EIF. Cette maladie appartient à la famille des leucodystrophies.
Comment dépister une leucopathie vasculaire ?
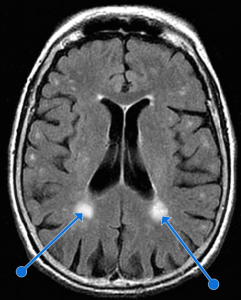
Les examens d’imagerie cérébrale (IRM, scanner) permettent de mettre en évidence les leucopathies. Le scanner est moins sensible que l’IRM, mais peut détecter des lésions étendues de la substance blanche. Ces leucopathies se traduisent alors par des lacunes (petites cavités qui reflètent des lésions du système nerveux central), des petits saignements et un dommage des capsules externes de la substance blanche.
Les leucopathies touchent en général les personnes présentant des facteurs de risque vasculaire (avec un risque de démence vasculaire), ayant des problèmes cardio-vasculaires ou souffrant athérosclérose. Ce sont, par exemple, des personnes diabétiques, hypertendues et souffrant d’hypercholestérolémie.
Les tests cognitifs (ex. : MoCA, MMSE) explorent les troubles attentionnels et mnésiques souvent présents dans la leucopathie vasculaire.
Il peut arriver que des individus exempts de toutes maladies décrites ci-dessous et âgées de moins de 50 ans présentent une leucopathie. Dans ce cas, le diagnostic s’orientera vers une maladie génétique de type leucodystrophie, également appelé leuco-encéphalopathie génétique.
Les leucoencéphalopathies d’origine génétique regroupent des maladies héréditaires caractérisées par une affection de la substance blanche :
- les leucoencéphalopathies vasculaires telles que la maladie de CADASIL et l’amyloïdose cérébrale familiale.
- Le syndrome childhood ataxia with Central nervous system hypomyelanisation.
- Le syndrome de l’X fragile avec des troubles précoces de la marche.
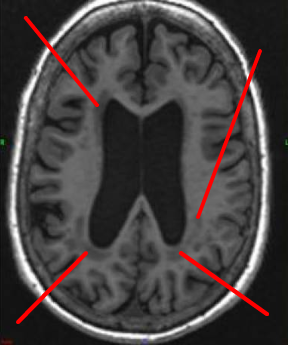
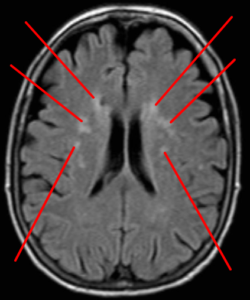
Les maladies inflammatoires ou infectieuses (p.ex. lupus, VIH, etc.) peuvent provoquer des leucopathies vasculaires.